
Historisch gesehen galten Oktopusse als Einzelgänger und asoziale Tiere (Barbato et al., 2007; Hanlon und Messenger, 2018). Neuere Studien deuten jedoch darauf hin, dass Oktopusse eine einzigartige und systematische Anordnung visueller Signale nutzen, um mit Artgenossen zu kommunizieren (Huffard, 2007; Caldwell et al., 2015; Scheel et al., 2016). Zu diesen visuellen Signalen gehören Farb- und Texturveränderungen, Körperhaltungen, verschiedene Fortbewegungsarten und Tintenmarkierungen, die kombiniert oder nacheinander eingesetzt werden können, um spezifische Signale zu erzeugen.
Zu den komplexesten Signalen, die Oktopusse nutzen, gehören Farbsignale. Da Oktopusse die Pigmentzellen, sogenannte Chromatophoren, direkt neuronal steuern, können sie Farbsignale schnell verändern, deren Stärke anpassen und sogar bilateral kommunizieren (Barbato et al., 2007; Hanlon und Messenger, 2018). Obwohl Oktopusse farbenblind sind, besitzen sie ein ausgezeichnetes Sehvermögen. Durch die Verwendung kontrastreicher Farbsignale können sie daher ihre Absichten (z. B. Dominanz oder Unterwürfigkeit) gegenüber Artgenossen deutlich zum Ausdruck bringen (Tricarico et al., 2011; Hanlon und Messenger, 2018).
Viele visuelle Signale, die Oktopusse nutzen, sind artspezifisch. Daher liefert die Charakterisierung und Dokumentation dieser Signale mittels Ethogrammen wertvolle Zusatzinformationen zur Bestätigung der Artbestimmung (Barbato et al., 2007; Huffard, 2007). Ethogramme sind nützliche Informationssammlungen, die das Verhalten von Organismen dokumentieren. Im Fall von Oktopussen können Ethogramme Wissenschaftlern als Ressource dienen, die untersuchen, wie ökologische Einflüsse, wie beispielsweise Interaktionen mit Artgenossen oder die Verfügbarkeit von Lebensraum, die Evolution der Signalentwicklung oder -kommunikation beeinflussen.

Der Rotaugen-Oktopus (Octopus rubescens) ist eine im Subtidalbereich beheimatete Art entlang der Westküste Nordamerikas (von Alaska bis Kalifornien). Er sucht Schutz in Kelpwäldern und felsigen Gebieten und ist häufig in der Admiralty Bay im US-Bundesstaat Washington anzutreffen (Cowles, 2005). Der Meeresboden dieser Bucht ist im Allgemeinen karg und flach und besteht aus Schlamm, Sand und kleinen Steinen. Für diese nicht grabende Oktopusart gibt es nur wenige Versteckmöglichkeiten. Die Bucht ist jedoch mit weggeworfenen Glasflaschen übersät, die O. rubescens opportunistisch als Höhlen nutzt (Anderson et al., 1999). O. rubescens hat diese neue Lebensraumquelle für sich entdeckt, was möglicherweise unbeabsichtigt zu einer Konzentration der Art in der Bucht geführt hat (Chase und Verde, 2011). Folglich interagieren O. rubescens in dieser „künstlichen“ Umgebung möglicherweise häufiger mit Artgenossen. Diese Interaktionen könnten durch visuelle Signale gekennzeichnet sein, die Oktopusse zur Kommunikation untereinander verwenden.
Da Oktopusse visuelle Signale zur Interaktion nutzen, war das Ziel dieser Studie, die Häufigkeit solcher Signale zu bestimmen, die von O. rubescens- Individuen zur Kommunikation mit Artgenossen verwendet werden, und diese visuellen Signale in einem Ethogramm zu dokumentieren. Daher befasste sich diese Studie mit den folgenden Fragen:
1) Welche visuellen Signale verwendet O. rubescens bei Interaktionen mit Artgenossen?
2) Wird die Häufigkeit der Interaktionen vom Geschlecht der Oktopusse beeinflusst?
3) Unterscheiden sich Art und Häufigkeit der visuellen Signale zwischen Initiatoren und Reaktoren einer Interaktion?
Methoden
Exemplare von Octopus rubescens wurden mittels Tauchen in der Admiralty Bay, Washington, gesammelt und im Rosario Beach Marine Laboratory (RBML), Anacortes, Washington, untergebracht. Die einzelnen Oktopusse wurden in Plastikbehältern mit konstantem Durchfluss von Meerwasser über ein Verteilersystem gehalten (Abbildung 1). Steine wurden auf die Behälter gelegt, um ein Entkommen der Oktopusse zu verhindern. Die Gesamtstichprobe (N) für dieses Experiment umfasste 20 Oktopusse (10 Männchen und 10 Weibchen).

Abbildung 1. Kunststoffbehälter mit konstantem Durchfluss von Umgebungs-Meerwasser (über ein Verteilersystem), in denen einzelne Oktopusse untergebracht waren; das System wurde von Chase und Verde (2011) entworfen und hergestellt.
Zur Identifizierung der visuellen Signale von O. rubescens wurden mit GoPro-Kameras (Abbildung 2) Videos von Oktopussen aufgenommen, die 15 Minuten lang in einem Beobachtungsbecken (Abbildung 3) interagierten.

Abbildung 2. Hergestellte Plexiglasrahmen (A), mit denen Kameras (B) an den Ecken des Beobachtungsbeckens befestigt wurden.

Abbildung 3. Versuchsaufbau: Ein Durchfluss-Meerwasserbecken wurde mit drei GoPro-Kameras (rote Kreise) ausgestattet. Das Becken war durch eine Plexiglasscheibe (größeres, gelbes Rechteck) mit Bohrungen zur Dämpfung der Wellenbewegung des ein- und ausströmenden Meerwassers (grünes Oval) unterteilt. Nur eine Hälfte des Beckens diente als Testbereich für die Oktopusse. Um tote Winkel für die Eckkameras im Becken zu vermeiden, wurden zwei Plexiglasscheiben zugeschnitten und quer zu den Beckenwänden angewinkelt, um den Raum zu verengen (kleinere, orange Rechtecke).
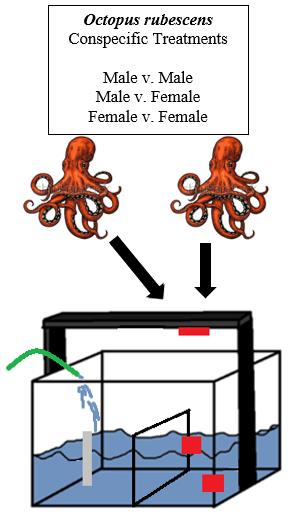
Jedem Oktopus wurde die Interaktion mit allen anderen Oktopussen des gleichen und des anderen Geschlechts gestattet (Abbildung 4).
Der VLC Media Player wurde zur Beobachtung und Analyse der von den GoPro-Kameras aufgenommenen Videos verwendet. Aus den Videos wurden Standbilder erstellt, um ein Ethogramm zu generieren. Jede Interaktion der Oktopusse, die mindestens 5 Sekunden dauerte, wurde hinsichtlich der Verwendung visueller Signale (Farbe, Textur, Fortbewegung und Körperhaltung) analysiert.
Ergebnisse
Während der 15-minütigen Versuche nutzte Octopus rubescens verschiedene visuelle Signale zur Kommunikation und Interaktion mit Artgenossen. Zu diesen visuellen Signalen zählten Farbsignale (Abbildungen 5 und 6), Textursignale (Abbildung 7), Tintensignale (Abbildung 8), Bewegungssignale (Abbildung 9) und Haltungssignale (Abbildung 10). Die Interaktionshäufigkeit unterschied sich um eine Interaktion pro Test zwischen den Kombinationen männlicher und weiblicher Oktopusse (5,2 Interaktionen pro Test) und den Kombinationen männlicher und weiblicher sowie weiblicher Oktopusse (4,2 Interaktionen pro Test).
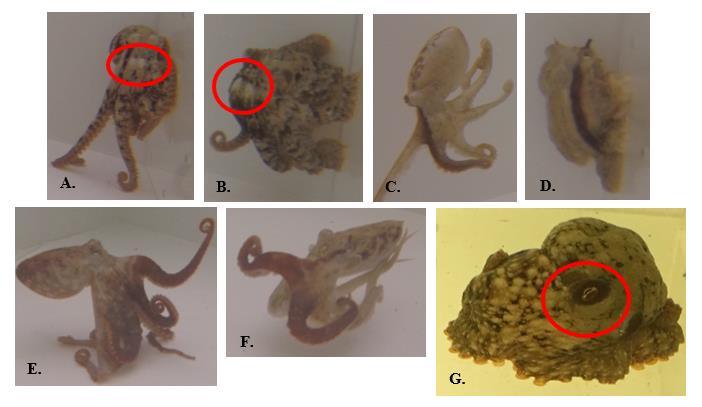
Abbildung 5. Farbsignale einzelner Körperteile von O. rubescens. A.–B. Falsche weiße Augenflecken: zwei benachbarte weiße Flecken unterhalb der Augen; C.–D. Dunkler Längsstreifen: verläuft typischerweise vom Auge entlang des ersten linken und/oder rechten Arms; erstreckt sich nicht immer über die gesamte Armlänge; E.–F. Dunkle Arme: typischerweise der erste linke oder rechte (oder beide) Arm des Oktopus; alle Arme können dunkel gefärbt sein; G. Dunkle Augenringe: dunkler Bereich um die Augen.

Abbildung 6. Ganzkörper-Farbsignale von O. rubescens. A. Hell: Körper hellocker bis grau oder weiß; B.–C. Gefleckter Ocker: ocker-/sandfarbener Körper; weiße und/oder braune/schwarze Flecken (Fleckendichte und -farbe variieren) über den gesamten Körper; D. Dunkelocker: vollständig verdunkelter Körper, rot bis braun/dunkelocker; E.–F. Deimatisch: dunkle Flecken/Flecken auf dem Mantel, helle Arme; G. Ocker: ocker-/sandfarbener Körper (etwas Variation in der Dunkelheit); H.–J. Intensiv gefleckt: starker Kontrast zwischen dunklen und hellen Zeichnungen auf dem Körper, dunkle Streifen/Bänder entlang der Arme können vorhanden sein; oft papillös.
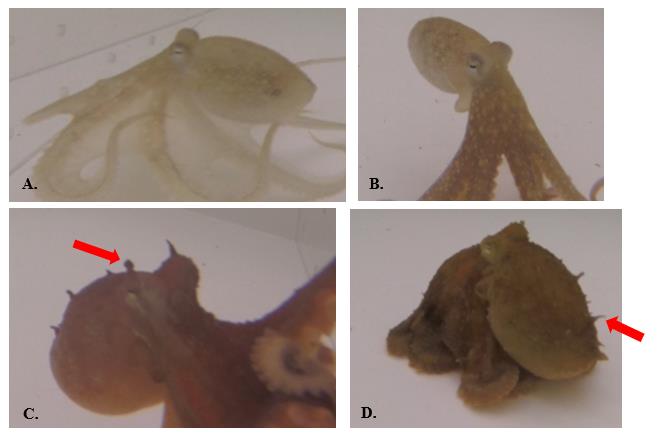
Abbildung 7. Textursignale, die von O. rubescens verwendet werden. A.-B. Glatt: keine Papillen; C.-D. Papilliert: Papillen sichtbar erhaben.

Abbildung 8. Tintensignal, das von O. rubescens verwendet wird. Das Tintensignal wurde als vorhanden oder nicht vorhanden erfasst.

Abbildung 9. Fortbewegungssignale von O. rubescens. A. Angriff: Der Oktopus stürzt sich auf einen Artgenossen; Vorwärtssturm; häufig wird der Rückstoßantrieb genutzt. B.–C. Ringen: Oktopusse verheddern sich in den Armen des anderen und greifen, beißen und packen. Nicht dargestellte Signale: Stillstand, Drohung, Flucht, Verfolgung, Annäherung.

Abbildung 10. Körperhaltungssignale von O. rubescens. A. Arme spreizen: Arme ausgestreckt; B. Abgeflacht: nah am Körper, Mantel gesenkt; C. Schnabel an Schnabel: Oktopusse stehen sich gegenüber und berühren sich mit den Schnäbeln; D. Greifen: Ein oder mehrere Arme strecken sich nach einem Artgenossen aus; E. Aufrecht: aufmerksam gegenüber einem Artgenossen; F. Stoßen: Arme zusammen, können aber auch eingerollt sein; G: Lose Arme: Arme hängen locker um/unter dem Körper, können leicht eingerollt sein; H. Aufrecht stehen: aufrecht, Arme gestreckt, um größer zu wirken; I. Ringen: Oktopusse kämpfen; J. Angriff: Arme zum Angriff auf einen Artgenossen bereit (die beiden vorderen Arme sind typischerweise eingerollt und hochgehalten); oft kombiniert mit dem Farbsignal „Verdunkelte Arme“; K. Arme erhoben: Arme erhoben, oft eingerollt; typischerweise die vorderen Arme; L. Kriechen: Arme ausgestreckt, locker oder eingerollt, treiben den Oktopus an. M. Angezogene Arme: Arme eng an den Körper angezogen.
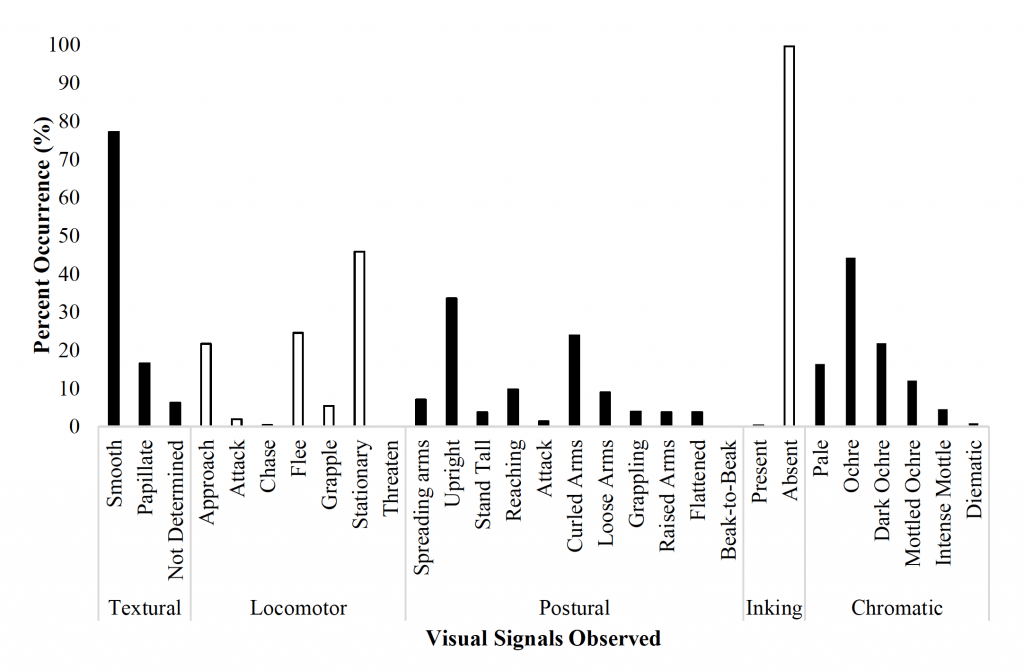
Abbildung 11. Prozentuale Häufigkeit der häufigsten visuellen Signale, die O. rubescens während der Interaktion mit Artgenossen in einem Beobachtungsbecken zeigt (N<sub>Männchen</sub> = N<sub>Weibchen</sub> = 10). Die fünf Signalkategorien umfassen Textur-, Lokomotions-, Haltungs-, Tinten- und Farbsignale, die jeweils verschiedene Unterkategorien aufweisen.
Die Interaktionen der Oktopusse (Abbildung 11) waren typischerweise durch die Bewegungssignale „stationär“ (45,9 %), „Annäherung“ (21,7 %) und „Flucht“ (24,6 %) gekennzeichnet, die von einem oder beiden Oktopussen in allen Geschlechterkombinationen (M/M, M/W, W/W) gezeigt wurden. Die häufigsten Farbsignale waren „ockerfarben“ (44,3 %), „dunkelockerfarben“ (21,9 %) und „hell“ (16,4 %); Oktopusse schienen „ockerfarben“ vorwiegend als Ruhefärbung zu verwenden. Die häufigsten Körperhaltungen waren „aufrecht“ (33,6 %) und „eingezogene Arme“ (23,9 %). Die Textursignale waren überwiegend „glatt“ (77,2 %), und Oktopusse färbten sich selten ein.
Die Interaktionen zwischen den Oktopussen wurden ebenfalls in Initiator und Reaktor innerhalb jeder Geschlechtskombination (M/M, M/F, F/F) unterteilt; diese Ergebnisse können im vollständigen Manuskript eingesehen werden, das über einen Link am Ende dieses Beitrags bereitgestellt wird.
Diskussion
Das in dieser Studie erstellte Ethogramm zeigt verschiedene visuelle Signale, die O. rubescens bei Interaktionen mit Artgenossen einsetzte, und deutet auf Kommunikation zwischen den Individuen hin. Die Anzahl der Interaktionen pro Test war für alle Geschlechtskombinationen (M/M, M/W, W/W) der Oktopusse ähnlich, was darauf schließen lässt, dass das Geschlecht nur geringen Einfluss auf die Häufigkeit der Interaktionen hatte. Obwohl sich O. rubescens möglicherweise aufgrund bestimmter Habitatressourcen, wie beispielsweise der als Höhlen genutzten Flaschen in der Admiralty Bay, in einem Gebiet versammeln, zeigte die Art in dieser Studie überwiegend aggressives Verhalten gegenüber Artgenossen. Dies legt nahe, dass sie keine soziale Art ist, auch wenn sie nicht einzelgängerisch lebt.

Dennoch sind visuelle Signale für Oktopusse in aggressiven Auseinandersetzungen besonders wichtig, da sie die Absicht eines Oktopus, anzugreifen oder sich zu unterwerfen, je nach Erfolgsaussichten deutlich zeigen können (Barbato et al., 2007; Scheel et al., 2016). Die Fähigkeit, diese Absicht auszudrücken, hilft Oktopussen, unnötigen Schaden zu vermeiden.
Ein aggressives Signal, das „Ringen“, trat zwar seltener auf als andere Haltungs- oder Bewegungssignale, kam aber dennoch während Interaktionen vor, am häufigsten zwischen Männchen. Die erhöhte Aggressivität zwischen Männchen könnte möglicherweise auf ihren Konkurrenzkampf um Weibchen in ihrem natürlichen Lebensraum zurückzuführen sein.
 Obwohl die dokumentierten Verhaltensweisen unter Laborbedingungen beobachtet wurden, kann das in dieser Studie erstellte Ethogramm dennoch als nützliche Referenz dienen. Zukünftige Studien können die visuellen Signale von O. rubescens aus anderen Lebensräumen erfassen und mögliche Variationen der von dieser Art verwendeten visuellen Signale aufdecken. Da die in dieser Studie verwendeten Oktopusse aus einer Population in der Admiralty Bay stammen, könnten diese Tiere im Gegensatz zu eher einzelgängerischen Oktopussen ein spezialisiertes System visueller Signale während Interaktionen nutzen. Dies könnte Wissenschaftlern die Hypothese ermöglichen, dass die von O. rubescens verwendeten visuellen Signale von umgebenden Lebensräumen wie der Admiralty Bay oder der Populationsdichte beeinflusst werden. Das in dieser Studie erstellte grundlegende Ethogramm kann zudem als zusätzliche Vergleichsgrundlage zwischen Oktopusarten dienen, unabhängig davon, dass die identifizierten visuellen Signale während Interaktionen mit Artgenossen erfasst wurden.
Obwohl die dokumentierten Verhaltensweisen unter Laborbedingungen beobachtet wurden, kann das in dieser Studie erstellte Ethogramm dennoch als nützliche Referenz dienen. Zukünftige Studien können die visuellen Signale von O. rubescens aus anderen Lebensräumen erfassen und mögliche Variationen der von dieser Art verwendeten visuellen Signale aufdecken. Da die in dieser Studie verwendeten Oktopusse aus einer Population in der Admiralty Bay stammen, könnten diese Tiere im Gegensatz zu eher einzelgängerischen Oktopussen ein spezialisiertes System visueller Signale während Interaktionen nutzen. Dies könnte Wissenschaftlern die Hypothese ermöglichen, dass die von O. rubescens verwendeten visuellen Signale von umgebenden Lebensräumen wie der Admiralty Bay oder der Populationsdichte beeinflusst werden. Das in dieser Studie erstellte grundlegende Ethogramm kann zudem als zusätzliche Vergleichsgrundlage zwischen Oktopusarten dienen, unabhängig davon, dass die identifizierten visuellen Signale während Interaktionen mit Artgenossen erfasst wurden.
Link zum vollständigen Manuskript – PDF herunterladen
Zitierte Literatur
Anderson, R., P. Hughes, J. Mather und C. Steele, C. 1999. Bestimmung der Ernährung von Octopus rubescens Berry, 1953 (Cephalopoda: Octopodidae) durch Untersuchung seiner Bierflaschenhöhlen im Puget Sound. Malacologia, 41:455–460.
Barbato, M., M. Bernard, L. Borrelli und G. Fiorito. 2007. Körpermuster bei Kopffüßern: „Polyphenismus“ als Form des Informationsaustauschs. Pattern Recognition Letters, 28:1854–1864.
Caldwell, R., R. Ross, A. Rodaniche und C. Huffard. 2015. Verhalten und Körpermuster des Großen Pazifischen Streifenoktopus. PLoS One, 10: e0134152.
Chase, E. und A. Verde A. 2011. Populationsdichte und Wahl des Baus und der Nahrung bei Octopus rubescens, gesammelt in der Admiralty Bay, Washington, im Juli 2011. American Academy of Underwater Sciences, 30:110–116.
Cowles, D. 2005. Octopus rubescens Berry, 1953
Hanlon, R. und J. Messenger. 2018. Cephalopod Behaviour. Cambridge (England): Cambridge University Press.
Huffard, C. 2007. Ethogramm von Abdopus aculeatus (D'Orbigny, 1834) (Cephalopoda: Octopodidae): Können Verhaltensmerkmale die Taxonomie und Systematik der Octopodiden beeinflussen? Journal of Molluscan Studies, 73:185–193.
Scheel, D., P. Godfrey-Smith und M. Lawrence. 2016. Signalverwendung bei Oktopussen in agonistischen Interaktionen. Current Biology, 26:1–6.
Tricarico, E., L. Borrelli, F. Gherardi und G. Fiorito. 2011. Ich kenne meinen Nachbarn: Individuelle Erkennung bei Octopus vulgaris. PLoS One, 6: e18710.
Autoren: Rachel L. Borisko, Kirt L. Onthank, E. Alan Verde





